
①提取药汁方法与实验室分离固液混合物操作相似,该操作的名称是,其中玻璃棒的作用是。
②下列哪位科学家(填字母)受启发,成功提取出抗疟新药青蒿素,获诺贝尔奖。
a. 拉瓦锡 b.屠呦呦 c.侯德榜 d.张青莲
臭氧(其化学式为O3)原本是大气中自然产生的一种具有特殊臭味的微量气体。在常温常压下可缓慢反应转化为氧气,当温度达到165℃迅速反应。臭氧量往往随纬度、季节和天气等因素的变化而不同。研究人员发现,天空中的臭氧层能吸收99%以上的太阳紫外线,为地球上的生物提供了天然的保护屏障。为何它又成了危害健康的污染物?
地表臭氧并非自然产生,主要是由石油产品(如汽油)等矿物燃料燃烧产生的氮氧化物与空气中的氧气结合而形成的。强烈的阳光照射会加速这一化学反应。地表空气中的臭氧对人体极为有害,一些易于过敏的人长时间暴露在臭氧含量超过每立方米180微克的环境中,会产生不良症状。研究表明,空气中每立方米臭氧含量增加100微克,人的呼吸功能就会减弱3%。
自2013年中国执行新《环境空气质量标准》,监测6种污染物以来,臭氧便成为一些城市夏季空气质量“超标日”的首要污染物。如图为某地夏季某日昼时(7:00~18:00)臭氧、二氧化氮(NO2)浓度随时间的变化图。
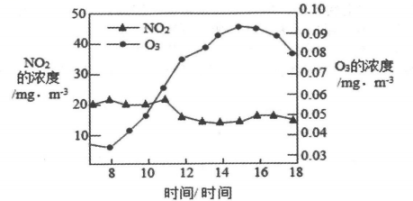
依据文章内容,回答下列问题。
I.气体的制取实验
图1 
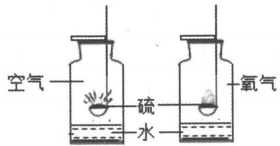 图3
图3 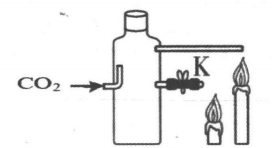
已知:水中加入的NaOH只起增强导电性作用,本身不参与反应。
图1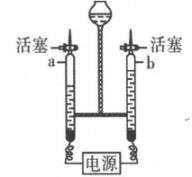 图2
图2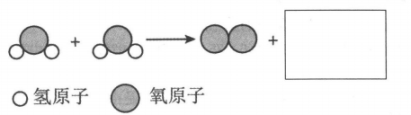
①据图可知,a管与电源的(选填“正”或“负”)极端相连。
②a、b两支玻璃管中生成气体的体积比约为。
③切断电源后,用燃着的木条在b玻璃管尖嘴口检验产生的气体,观察到的现象是。
图3 图4
图4
①上述反应的化学方程式为。
②该实验(填“能”或“否”)说明水的元素组成。
①上述实验中,电解水速率最快的条件是NaOH溶液、电压V。
②电解溶质质量分数为5%的NaOH溶液时,改变电压对电解水速率的影响是。
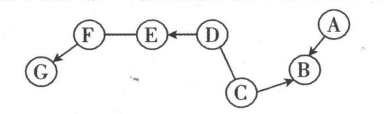
①写出A的名称:。
②写出铁丝和B反应的化学方程式:。
③C和D发生化学反应的过程(填“吸热”或“放热”)。
④写出E和F反应的化学方程式:。
⑤若G能与血红蛋白结合导致人体中毒,则其化学式为。
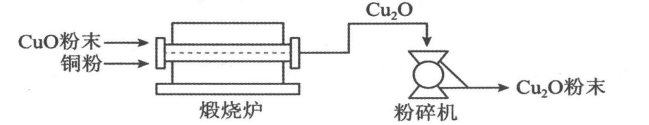
①800~900℃时,煅烧炉中发生化合反应,该反应的化学方程式为。
②粉碎机中,发生的变化属于(填“物理变化”或“化学变化”)。